兰卫医学助力客户登顶《Immunity》:揭秘肺部共生真菌诱发肺纤维化的新机制
肺纤维化(Pulmonary Fibrosis, PF)是一种以肺间质进行性瘢痕形成为特征的致死性呼吸系统疾病,其细胞外基质的过度沉积会严重损害患者的肺部结构与呼吸功能。既往研究表明,肺泡巨噬细胞(alveolar macrophages, AMs)的异常活化在纤维化发生发展中发挥关键作用,可通过促进成纤维细胞增殖与活化,加速病理进程。
C型凝集素受体(C-type lectin receptors, CLRs)主要表达于髓系细胞表面,是调控肺部免疫应答的重要模式识别受体。其中,Dectin-1(基因:CLEC7A)作为识别真菌β-葡聚糖的关键模式识别受体,在肺部抗真菌免疫中占据重要地位。肠道共生真菌已被证实可影响炎症反应,然而肺部常驻共生真菌群落在PF发生发展中所扮演的具体角色,仍知之甚少。特别是,肺部共生真菌是否通过Dectin-1介导AMs发生免疫代谢重编程,从而驱动其向促纤维化表型转化,这一机制链条尚缺乏系统性研究。
兰卫医学科研团队协助深圳市儿童医院研究团队系统解析了真菌微生态与免疫代谢互作在肺纤维化中的调控作用。该研究以《Dectin-1 facilitates lung fungal-mediated pulmonary fibrosis》为题发表于国际期刊《Immunity》,为理解PF的免疫机制提供了新的理论依据。

一、核心发现与机制概述
研究团队取得了突破性发现:肺部共生真菌是推动肺纤维化的重要“幕后推手”,而Dectin-1则是关键的“信号放大器”!
核心机制概述:在肺纤维化发生时,一种特定的肺部共生真菌(Engyodontium)通过结合AMs表面的Dectin-1受体,激活了下游的Raf1信号通路(值得注意的是,这一过程竟然绕过了经典的CARD9通路)。这一信号级联反应促使原本处于“静息状态”的AMs发生“黑化”,转变为促纤维化表型(大量分泌Arginase-1和TGF-β)。这些促纤维化因子随后激活了成纤维细胞,最终导致严重的肺纤维化。
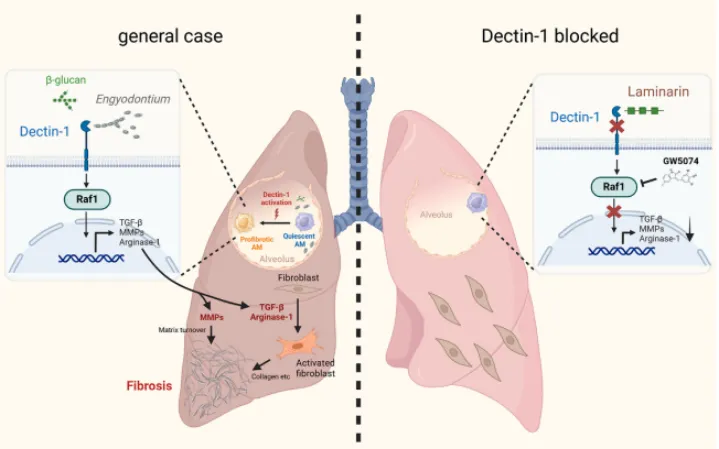
研究结论示意图
二、研究思路

三、研究过程与实验结果解析
1.临床现象与基因敲除验证:Dectin-1是纤维化的“帮凶”
为系统评估CLRs在肺纤维化中的作用,研究者首先分析了人类IPF患者scRNA-seq数据(GSE157691),发现CLEC7A在CLRs家族中表达最为显著,并特异性富集于AMs。其表达不仅在IPF肺组织中显著上调,还与AMs标志基因MRC1及多种胶原和纤维化相关基因呈正相关关系。在博来霉素(BLM)诱导的小鼠肺纤维化模型中,Clec7a在静息及活化AMs中均明显升高,并与纤维化相关基因表达谱一致。功能研究表明,Dectin-1缺失(Clec7a−/−)可显著缓解BLM诱导的肺纤维化,表现为生存率提高、胶原沉积减少及组织结构损伤减轻。转录组与单细胞分析进一步揭示,Clec7a缺失抑制了促纤维化AMs相关基因表达,同时下调TGF-β信号通路及细胞外基质相关基因集。分选AMs结果亦证实Arg1和Tgfb1表达降低。这提示Dectin-1在肺纤维化进程中发挥关键调控作用。
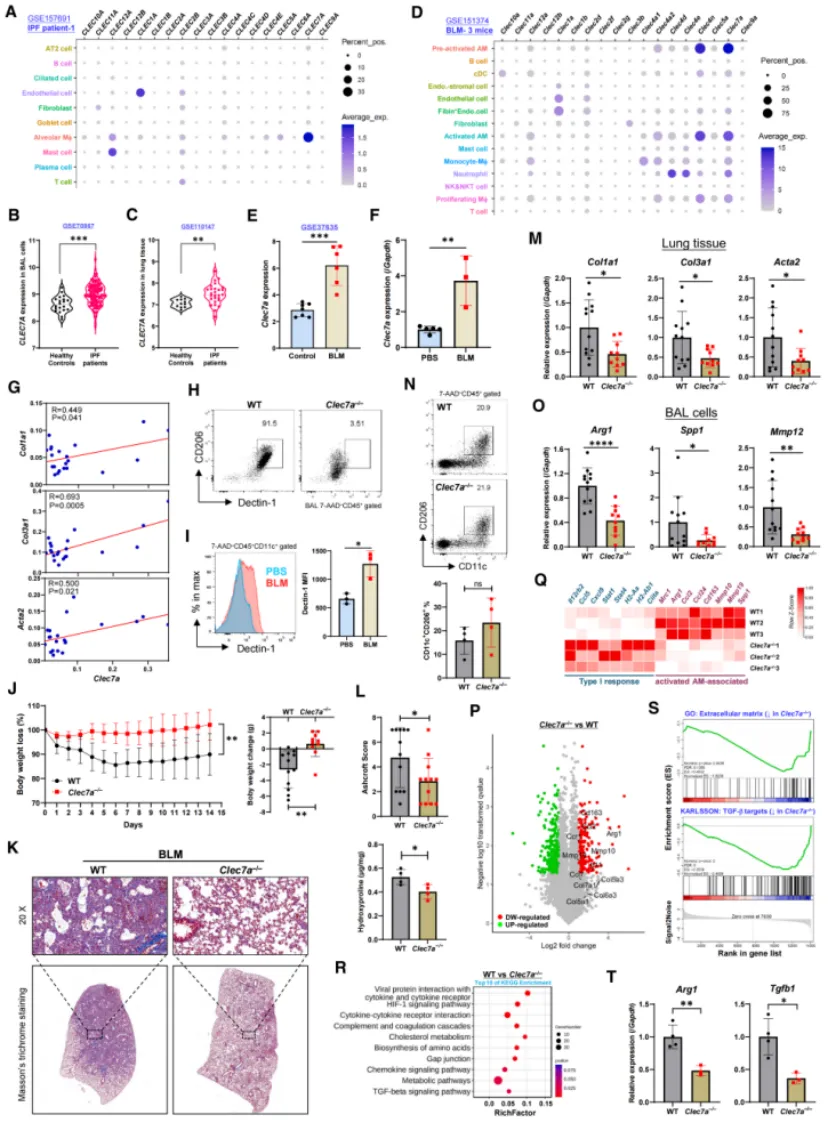
图 Dectin-1敲除显著逆转肺纤维化进程
2.细胞命运追踪:Dectin-1驱动巨噬细胞“促纤转化”
scRNA-seq和巨噬细胞转移实验揭示,在纤维化过程中,静息状态的肺泡巨噬细胞需要依赖Dectin-1信号,才能“转型”为高表达Arginase-1和TGF-β的促纤维化巨噬细胞。如果使用Dectin-1拮抗剂(Laminarin),则能有效阻断这一恶性转化。
3.揪出关键通路:依赖Raf1,而非CARD9
既往研究普遍认为,Dectin-1主要通过经典的CARD9通路介导下游信号转导。然而,本研究通过基因敲除验证发现,Card9缺失并未显著影响BLM诱导的肺纤维化进程,提示其在该疾病中的作用有限。相较之下,Dectin-1的另一下游分子Raf1在纤维化调控中发挥关键作用:无论采用Raf1抑制剂GW5074干预,还是在巨噬细胞中选择性敲除Raf1,均可显著减轻体重下降、胶原沉积及促纤维化基因表达,且该效应依赖于Dectin-1存在。此外,巨噬细胞耗竭与回输实验,以及与成纤维细胞的体外共培养研究进一步表明,阻断Dectin-1-Raf1信号轴可抑制成纤维细胞活化及纤维化相关基因表达。这些结果表明,在肺纤维化背景下,Dectin-1主要通过一条CARD9非依赖、Raf1依赖的非经典信号通路发挥作用,从而修正了既有认知,并揭示了新的关键调控机制。
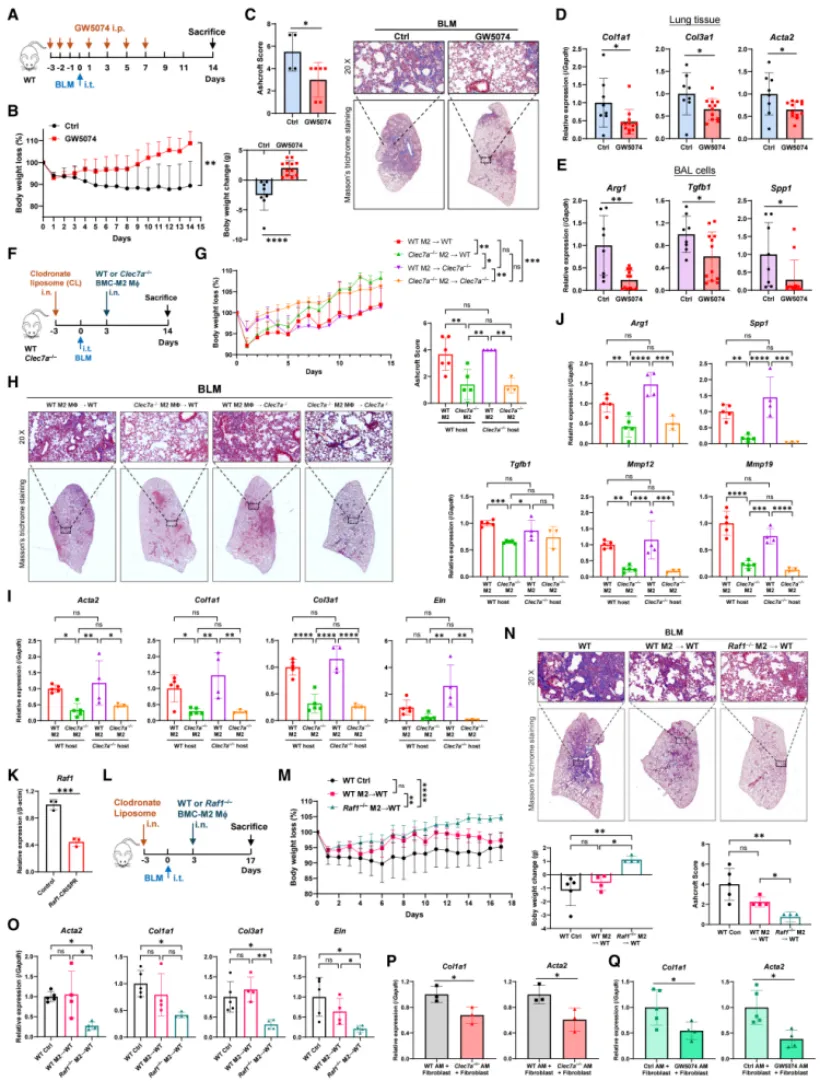
图 锁定Raf1!非经典通路的全新发现
4.锁定真凶:揪出肺部特异性共生真菌
为明确Dectin-1的功能性配体来源,研究者首先通过抗真菌药物氟康唑(FCZ)清除小鼠肺部真菌,发现可显著缓解BLM诱导的肺纤维化,包括体重下降减轻及促纤维化因子表达降低,而该效应在Clec7a−/−小鼠中消失,提示真菌作用依赖Dectin-1信号通路。进一步结合Dectin-1-Fc融合蛋白“垂钓”策略与ITS测序分析,鉴定出肺部共生真菌Engyodontium sp.可作为关键配体来源。功能验证表明,将该真菌重新定植于小鼠肺部后,可显著加重纤维化表型,且该效应依赖Dectin-1-Raf1信号轴,在Dectin-1缺失背景下不再出现。
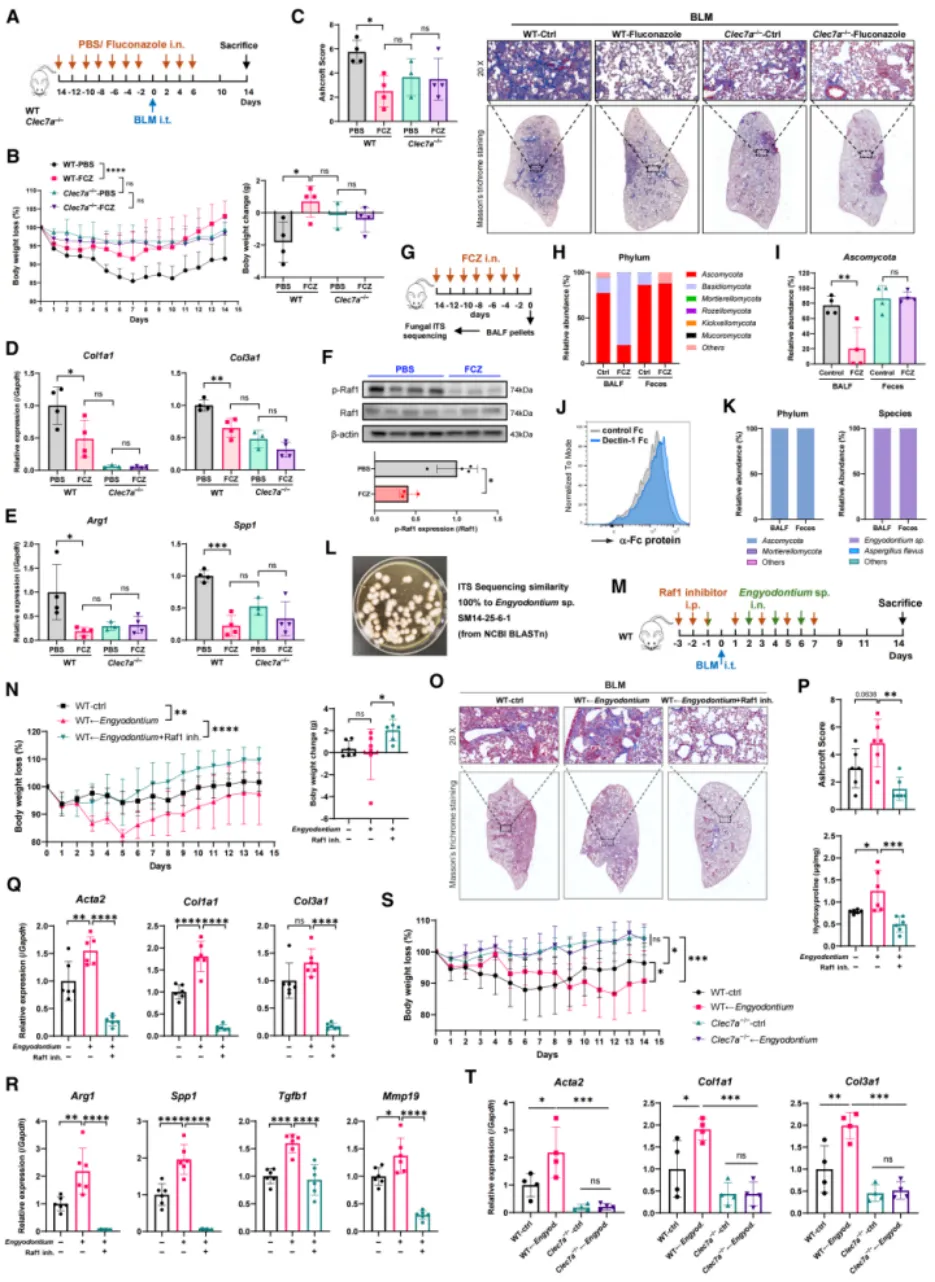
图 破案了!肺部共生真菌Engyodontium sp.现出原形
5.临床转化验证:在人类IPF样本中重现机制
在机制研究基础上,作者进一步在人类IPF样本中验证Dectin-1信号的临床相关性。组织学与免疫荧光结果显示,纤维化区域中DECTIN-1⁺CD206⁺AMs显著富集,并与α-SMA⁺成纤维细胞紧密接触,且DECTIN-1与RAF1在空间上共定位,提示该通路在人体内处于活跃状态。单细胞转录组与拟时序分析揭示,MRC1hi AMs逐步向SPP1⁺等促纤维化亚群转化,且CLEC7A与TGFB1表达呈正相关。功能上,IPF患者BAL细胞上清可显著诱导成纤维细胞中ACTA2、COL1A1等基因表达;Dectin-1激动剂Curdlan进一步增强该效应,而拮抗剂Laminarin或Raf1抑制剂GW5074则可有效阻断。体外实验亦证实,激活Dectin-1-Raf1通路可促进人源AMs获得促纤维化表型。
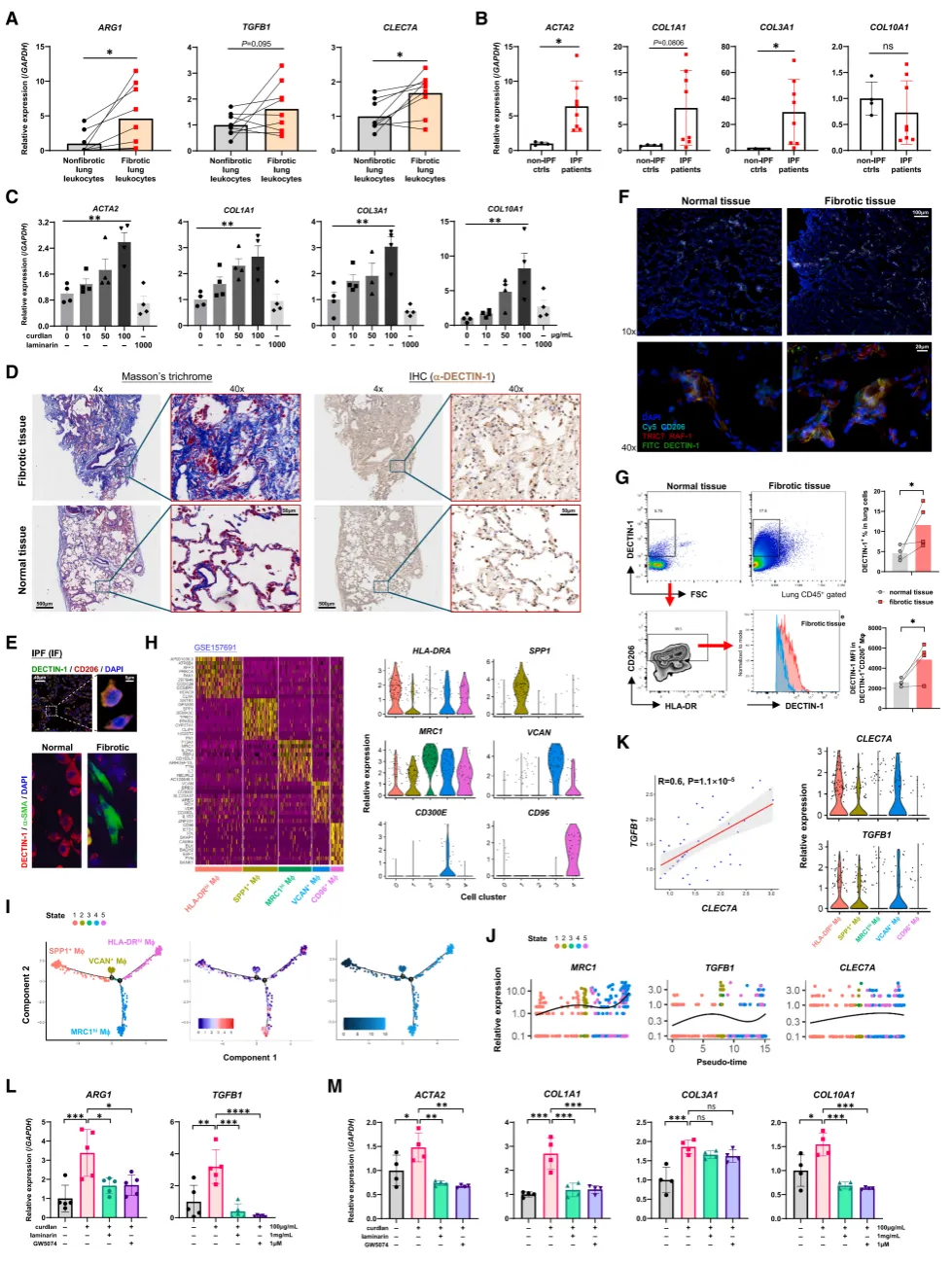
图 回归临床:在人类IPF患者中得到完美印证
四、优势与创新点
本研究首次明确“肺部局部共生真菌”在肺纤维化发生中的关键驱动作用,将研究视角拓展至肺部微生态,丰富了对疾病发生机制的整体认识。
机制创新
发现了Dectin-1在肺纤维化过程中并非依赖经典的CARD9通路,而是通过一条“CARD9非依赖、Raf1依赖”的非经典信号通路发挥作用,从而拓展了CLRs信号转导网络的理论体系。
转化潜力明确
在机制阐明的基础上,研究进一步提出了可行的干预方向,包括抗真菌治疗、Dectin-1拮抗剂(如Laminarin)以及Raf1靶向抑制剂等,为目前缺乏有效治疗手段的肺纤维化提供了具有潜力的全新治疗策略。

